▎药明康德内容团队编辑
今日,美国FDA宣布,批准Relyvrio(苯丁酸钠和牛磺酸二醇口服固定剂量配方)上市,用于治疗肌萎缩侧索硬化(ALS)。这款疗法的获批过程可谓一波三折。今年3月,FDA咨询委员会以6:4的投票结果,表示临床数据尚不支持这款疗法的有效性。之后,Amylyx公司递交了对临床试验数据的进一步分析以及来自其它临床试验的支持数据。AMX0035也首次获得加拿大监管机构的批准有条件上市。在今年9月召开的
第二次FDA咨询委员会
上,委员会成员以7:2的投票结果,支持这一疗法获得FDA批准。今天这一疗法终于成功冲过了终点线!
肌萎缩侧索硬化症(ALS)是一种进行性神经退行性疾病,影响大脑和脊髓中的神经细胞,也被称为“渐冻人症”。这种疾病的患者大脑和脊柱的运动神经元会不断死亡,导致患者的肌肉无力和瘫痪,从无法行走到无法说话、吞咽、呼吸。ALS患者在确诊后平均寿命只有四年。目前尚不清楚该病的确切发病机制。
Relyvrio是两种药物苯丁酸钠(sodium phenylbutyrate)和牛磺酸二醇(taurursodiol)的复方制剂。它们可以改善细胞内线粒体和内质网的健康状态,从而延缓神经细胞的死亡。临床前试验表明,这两种药物联用的协同效应,能够将神经细胞因为氧化应激而产生的死亡减少90%。FDA曾授予Relyvrio孤儿药资格和优先审评资格。
此次获批是基于一项入组了137例ALS患者的2期临床试验获得的积极数据。试验达到其主要疗效终点,即根据修订的ALS功能评定量表测量,在6个月随机化阶段结束时,接受Relyvrio治疗的ALS患者运动功能下降显著减缓。
此外,对所有随机化受试者长达3年的随访显示,在试验开始时就接受Relyvrio治疗的患者,与最初接受安慰剂治疗,在开放标签阶段转为Relyvrio治疗的患者相比,死亡风险降低了44%(HR 0.56;95% CI,0.34-0.92)。并且始终接受Relyvrio治疗组中位生存期比最初接受安慰剂治疗的患者组延长了6.5个月(25.0个月 VS. 18.5个月)。
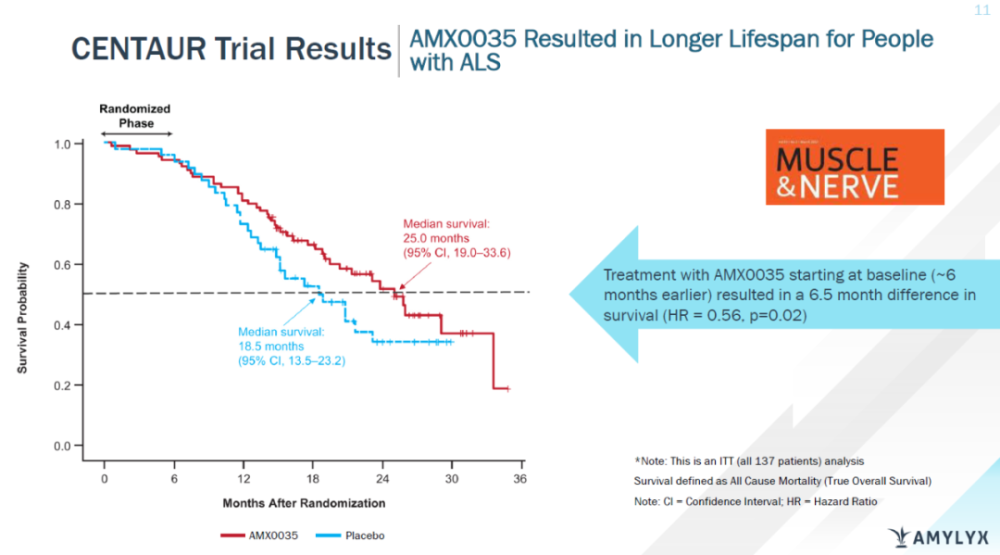
▲Relyvrio延长ALS患者生存期(图片来源:Amylyx公司官网)
安全性上,总体而言,在24周内,Relyvrio和安慰剂组之间报告的不良事件和停药率基本相似,但是Relyvrio组胃肠道事件的发生率更高。
“Amylyx的目标是让每个符合资格使用Relyvrio的病患能够以最快、最有效率的方式使用药物,因为我们知道ALS患者和他们的家人没有时间再等待,”Amylyx的共同首席执行官Joshua Cohen与Justin Klee先生说道,“我们的团队已经准备好帮助ALS患者取得这项重要的新治疗选择。”
ALS领域在近年来得到更多的关注和研发投入。根据药明康德内部数据库的统计,截至今年5月底,已有近百款ALS候选药物进入临床开发阶段。期待更多创新疗法研发顺利,早日来到患者身边。





















