胰腺导管腺癌是所有常见癌症中最致命的一种,常常在注意到症状时已是晚期,容易转移,并且现有的疗法包括免疫疗法对其没什么效果。解决这一难题的路径中,新型的T细胞受体基因疗法值得关注。
T细胞受体(TCR)基因疗法是利用患者自身的T淋巴细胞治疗癌症的前沿基因疗法。即对患者自身的T淋巴细胞在体外进行改造,然后将它们注回患者体内杀伤肿瘤。
最近新英格兰医学杂志报道了一例晚期转移性胰腺导管腺癌患者[1],接受了这种新型的T细胞受体基因疗法(以下简称TCR-T疗法),肿瘤大幅消退,疗效持久。
几经治疗,肿瘤仍在生长
患者是一位71岁的女性。她在67岁时被诊断为胰腺癌,此前她有胆道狭窄,并且胰腺炎反复发作。当时CA 19-9和其他肿瘤标志物的水平没有升高。
2018年,她接受了四个周期的FOLFIRINOX新辅助治疗(氟尿嘧啶、亮丙瑞林、伊立替康和奥沙利铂),随后进行了保留幽门的胰十二指肠切除术,切除了一个分化不良的腺癌(4.5cm,边缘阴性),以及21个淋巴结,其中有两个受累淋巴结。这次治疗后疾病分期为IIB(ypT3N1M0)。随后患者又接受了四个周期的辅助性FOLFIRINOX治疗,以及辅助性化放疗和卡培他滨治疗。在2019年之前患者一直保持无病状态。
2019年,患者右肺下叶发现一个增大的结节,通过细针抽吸活检证实存在肺部转移。不过腹腔盆腔没有出现疾病复发。
2020年,患者参加了匹兹堡大学医学中心的肿瘤浸润淋巴细胞治疗的临床试验(NCT03935893),接受了体外扩增的肿瘤浸润淋巴细胞和高剂量白细胞介素-2的治疗。不过,半年后肺部转移灶仍在生长。检测发现,患者肿瘤PD-L1的表达低于1%,肿瘤突变负荷为8.9个/Mb,微卫星稳定,存在KRAS G12D突变。此外没有检测到基因拷贝数变异或基因融合。患者HLA基因型为HLA-C*08:02。
新型TCR-T疗法
2021年5月,美国FDA批准了一项单患者研究性新药申请。2021年6月,患者接受了这种新型治疗。
首先,分离出患者外周血里的T细胞,经过体外处理和改造,这些T细胞上的受体能够特异性地识别KRAS G12D突变。
在细胞输注前五天,患者开始使用免疫抑制剂托珠单抗(600mg,静脉注射)和环磷酰胺(每天每公斤体重30mg,静脉注射2天)。使用免疫抑制剂的目的在于避免输注免疫细胞后发生细胞因子释放综合症。
接下来,患者输注了这些被改造的T细胞,其中包括85%的CD8+T细胞和15%的CD4+T细胞,前者能直接杀死肿瘤细胞,后者能起到助攻作用。大约91.5%的输注细胞表达能识别KRAS G12D突变的T细胞受体(图1)。
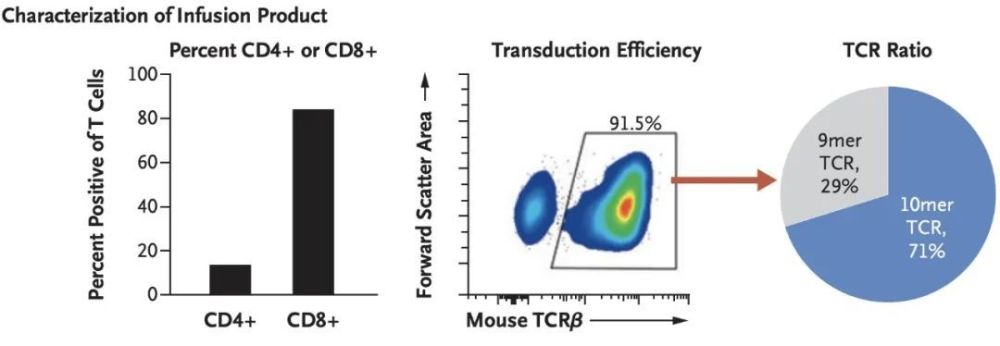
图1. 输注细胞的组成
在细胞输注后18小时,病人接受了高剂量的白细胞介素-2,目的是帮助这些输注的T细胞进行扩增。
患者出现了一些预期之内的短暂的毒性反应,比如环磷酰胺治疗带来的恶心和骨髓抑制,以及高剂量白细胞介素-2带来的低血压、转氨酶水平升高、发烧和疲劳。没有观察到额外的T细胞疗法的毒性反应。
患者在第11天出院,接下来作为门诊病人接受骨髓生长因子、血小板和红细胞的输注。在细胞输注后第21天,她的中性粒细胞数量已经恢复,血小板也在第28天恢复。
患者在2020年接受肿瘤浸润淋巴细胞治疗时,长期每天服用丝裂霉素后出现了直立性低血压,这一次也出现了,不过通过静脉输液和口服氟氢可的松(每天0.1毫克,共10天)得到了控制。
肿瘤持续缓解
细胞输注后一个月后,患者进行了首次随访。CT扫描显示,患者的肺部转移病灶出现了部分消退,反应率为62%。细胞输注后半年,肿瘤消退仍在继续消退,反应率为72%(图2)。

图2. 肺部转移病灶在治疗前、治疗后85和176天的CT影像
患者血清中效应T细胞细胞因子干扰素-γ、TNF、GM-CSF和CCL4的浓度在基线时较低,但在细胞输注后一天大幅增加并达到峰值(图3)。当病人在细胞输注后11天出院时,干扰素-γ的水平与基线相比仍然较高。在细胞输注后约一个月时,输注的T细胞约占循环中所有T细胞的13%,3个月时是3.3%,6个月时仍有2.4%,主要是CD8+细胞。

图3. 患者血清里免疫细胞因子变化情况
启示
该案例中的转移性胰腺癌患者,对标准疗法和肿瘤浸润淋巴细胞疗法没有反应。不过,通过对自身的T细胞进行改造,让它们能特异性识别KRAS G12D突变,再输注回体内杀死肿瘤细胞,效应强大持久。
不过,虽然这种疗法对于该病人疗效好,但是从成功的个例推广到普适的疗法,还有不少的工作要做。医生们还用同样的手段治疗了另一名患者,虽然有着类似的免疫反应,一个月后观察到了部分消退,但是这名患者在接受治疗半年后不幸去世。研究者们仔细检查了肿瘤的基因组特征,尚未发现是什么原因导致了治疗失败。
另外, TCR-T疗法取决于病人的特定HLA基因型。这个研究中使用的KRAS G12D特异性T细胞受体受限于HLA-C*08:02,也就是说,病人得表达该基因型才行。针对其他HLA基因型的基因治疗也正在研究中。
下一步是进行前瞻性的临床试验,以确定这种疗法在胰腺癌和其他有KRAS突变的癌症中的治疗潜力。让我们期待更多疗法的开发和更多患者的获益!